研究进展
研究进展
在超低场磁传感技术、分子和细胞的磁成像及相互作用等纳米生物技术研究领域做出了具有创新性的工作。通过高灵敏的光学原子磁力仪,开发磁性纳米颗粒物的定量成像技术和新型的磁基生物力学技术,探索力化学耦合调控抗菌抗肿瘤方面的基础研究。现已发表J. Am. Chem. Soc.、Angew. Chem. Int. Ed.、Adv. Mater.等SCI科研论文70余篇,授权中国发明专利10余项。
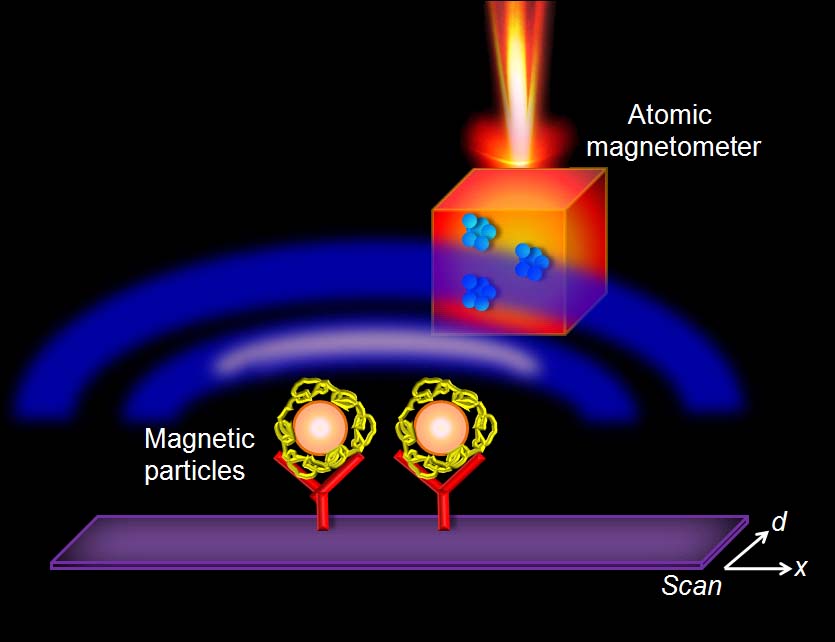
1)基于超灵敏光学原子磁力仪,开发了一种新型的扫描磁成像技术。
纳米磁颗粒物在生物医学上的广泛应用使得人们对磁颗粒物成像产生了极大的兴趣。这种新型的扫描磁成像技术可以在避免使用强磁场和接近室温的工作环境下,直接测量磁性纳米颗粒物产生的超弱磁场,在获得颗粒物定量信息的同时,也能得到空间成像信息,进而提供一种高分辨率和高灵敏度的纳米颗粒物成像技术,适合于多种生物医学的应用。研究结果于2009年发表在Angew. Chem. Int. Ed.上,并被Nature nanotechnology作为Research Highlights报道。
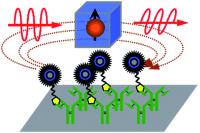
2)将这种新型的扫描磁成像技术应用于分子成像的研究。
当颗粒物表面被不同的生物分子修饰后,这些磁性粒子便可应用于生物传感器、磁分离技术、医疗成像、药物输送的载体等方方面面。在这些应用中,磁纳米颗粒物精确的定量和定位是至关重要的。在进一步实现了多个样品的二维磁成像之后,利用其高灵敏度和高分辨率的特性,开展了以抗体/抗原为代表的分子成像研究。这是一种新的磁免疫技术,提供了宝贵的定量成像信息,其实验检测限可与磁探测最灵敏的超导量子干涉仪(SQUID)相媲美。而检测距离能够更远,适用于更多的实际环境。研究成果于2010年发表在Angew. Chem. Int. Ed.上。
3)将扫描磁成像技术与外界微扰力相结合,进一步开发了力诱导的剩磁谱技术(FIRMS)。
将扫描磁成像技术与外界微扰力(包括离心、超声、微流控等)相结合,进一步开发了力诱导的剩磁谱技术(FIRMS)来探测生物分子间(抗体-抗原、受体-配体、DNA/RNA、蛋白质、酶)的相互作用。FIRMS技术不需要繁琐的物理分离,而是采用分子间特异的相互作用力来探测多种不同生物分子,其力谱的分辨率可以达到鉴别DNA单碱基对。同时,通过FIRMS技术还直接测量了凝血酶及其核酸适配体的多价态作用效应,开展了检测特异性靶细胞的工作,定量研究了CD3+T细胞表面的物理吸附和特异性吸附,这对分子识别和医学诊断具有重要的现实意义。研究结果发表于Angew. Chem. Int. Ed.、J. Phys. Chem. B、Chem. Eur. J.。
4)采用DNA-RNA双链分子间的相互作用力作为内标,构建新型的DNA机械传感装置。
生物体内的各种组织、器官乃至整个个体的运动最终都归结为分子马达在微观尺度上的运动。蛋白质合成过程中核蛋白体的移位需要马达蛋白EF-G的作用。利用FIRMS技术,我们测量了一系列DNA-RNA双链分子间的相互作用力。进而以分子间的相互作用作为参照力,构建新型的DNA机械传感装置,研究了马达蛋白EF-G所产生的动力冲程,成果于2013年发表在Angew. Chem. Int. Ed.上。
此外,通过利用机械力和DNA序列的双重调控能力,发展了一种新型的机械传感器,获得凝血酶蛋白8个数量级的动态检测范围,使检测限达到10fM,实现宽范围、高灵敏度的蛋白免标记检测,并研究了人端粒的G-四链体与Ku蛋白、mPDS配体的多元相互作用,确定了mPDS配体与蛋白协同作用范围,为抗肿瘤药物的筛选与评价提供了新的方法,研究结果选为期刊封面Anal. Chim. Acta 2019, 1045, 1。
将扫描磁成像技术与分子间的交换反应相结合,开发了一种新型的microRNA检测方法,交换诱导的剩磁谱技术(EXIRM)。miRNA是一类非编码的短链RNA 分子,调节着人类三分之一的基因。我们采用microRNA目标分子和磁标记分子之间的交换反应,利用原子磁力仪的超高灵敏度,能够实现zeptomole(10-21mol)量级的高灵敏度检测,避免了物理分离和放大技术的干扰,将适用于癌症早期诊断中microRNA的筛选。研究结果2013年发表于Chem. Commun.。
5) 设计制备具有级次结构的高性能纳米磁探针和磁材料
为满足深入开展超低场研究的需求,在建立和完善超低场磁成像和生物力谱特色综合研究平台的同时,设计制备多功能的超低场磁探针和磁材料,揭示其潜在的生物应用能力。设计合成了不同尺寸的磁性纳米粒子,并通过自组装方法,制备了一种性能优异的超低场磁探针,并且还具有载药、可控释放、遥感传输和精准定位多种生物医学功能,为超低场技术的实际应用开辟了新的道路(J. Am. Chem. Soc. 2016, 138, 2090)。采用"一锅法",通过自洽序列生长的方式,制备获得尺寸均一、高度结晶、结构完美的FePt@Fe3O4双磁性核壳结构纳米晶,避免使用预先合成的种子或者分步加热的繁琐过程;利用核壳结构界面处的晶格缺陷,产生强的交换耦合效应,显著提升探针磁性能(J. Am. Chem. Soc. 2019, 141, 3366)。
6) 提出基于力化学耦合调控的抗细菌粘附和抑制肿瘤转移的新策略
在上述力谱平台研发及高性能纳米磁探针研究基础上,进一步拓展细胞机械化学研究。我们采用基于纳米磁探针的超低场技术,建立了测定细胞粘附及迁移等机械性质的新方法,进行了细胞生物力学的安全评价,实现了肿瘤细胞的分型检测(Nanoscale 2020, 12, 14573)。并通过测量细菌与基质的粘附力,研究了基质硬度对细菌初始粘附的调控,首次报道细菌(S.aureus)粘附力与基质硬度之间存在良好正相关关系,其中S.aureus表面蛋白Fnbp发挥了关键性机械转导作用,这为基质硬度调控的抗菌材料设计提供了新思路(Nanoscale 2019, 11, 7648)。
肿瘤转移是癌症导致死亡的主要原因。而肿瘤转移的整个过程中,细胞粘附与迁移、细胞骨架、基质硬度等机械力因素发挥着重要的作用。通过超低场力谱研究发现抗紫杉醇的耐药细胞伴随着较强粘附和迁移的机械性质。我们采用光动治疗手段,调控胞外基质介导肿瘤细胞粘附,可使肿瘤细胞机械化学性质和粘附力显著下降,并降低细胞迁移和入侵能力,诱导细胞失巢性凋亡,增加治疗的敏感性,最终成功抑制肿瘤的转移,为抗肿瘤治疗提供了新的视窗(Biomaterials 2018, 173, 22)。